Aminosäuren

FERMOPURE® – pflanzenbasiertes L-Cystin und L-Cystein
Traditionell wird die Aminosäure L-Cystein und sein Dimer L-Cystin aus tierischen Ausgangsstoffen wie Federn oder Haaren gewonnen. WACKER ist weltweit das erste Unternehmen, das natürliches L-Cystin in einem nachhaltigen Fermentationsprozess herstellt. Diese patentierte Technik wurde 2008 mit einem Umweltpreis ausgezeichnet, da 96 % weniger Salzsäure verbraucht werden, als für die typische chemische Extraktion aus Haaren und Federn erforderlich ist. Das natürliche L-Cystin und das vegane L-Cystein von WACKER werden in modernsten Produktionsanlagen hergestellt, wodurch wir höchste Qualität erzielen. Seit 2019 werden die Produkte unter der Marke FERMOPURE® vertrieben.
Im Jahr 2018 wurde die Produktion an den spanischen Standort León verlagert. Dort produziert WACKER L-Cystin nach ISO 9001:2015 und den hohen Qualitätsanforderungen des FSSC 22000, einer von der GFSI (Global Food Safety Initiative) anerkannten Norm zur Gewährleistung der Lebensmittelsicherheit. Der Fermentationsstandort von WACKER in León verfügt über beide Zertifikate, um ein hohes Sicherheitsniveau unserer Produkte zu gewährleisten.
Produkt-Highlights:
Das patentierte biotechnologische Verfahren von WACKER kommt ohne tierische Produkte aus und reduziert den Einsatz von Salzsäure im Vergleich zu alternativen chemischen Extraktionsverfahren erheblich.
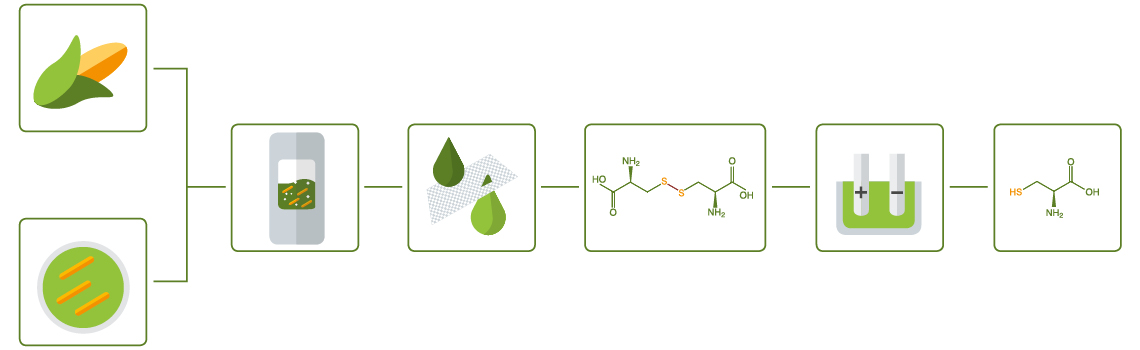
Pflanzenbasierte, nachwachsende Rohstoffe
Als Ausgangsmaterial für unseren Fermentationsprozess verwenden wir Glukose, die ausschließlich aus Pflanzenstärke gewonnen wird.
Mikroorganismen
Wir verwenden einen gut untersuchten Mikroorganismus, der von Natur aus in der Lage ist, L-Cystein zu synthetisieren. Der Stoffwechsel wurde auf maximale Effizienz optimiert.
Fermentation
Im Fermenter produzieren die Mikroorganismen in einem kontinuierlichen Strom L-Cystein aus Glukose und anorganischen Spurenelementen. Das Produkt wird in die Nährlösung abgegeben und kristallisiert unmittelbar zum Dimer L-Cystin aus.
Reinigung
Die Fermentationslösung wird aufgereinigt, um natürliches L-Cystin zu erhalten.
L-Cystin
L-Cystin ist ein Dimer, das aus zwei oxidierten L-Cystein-Molekülen besteht.
Elektrolyse
Zur Herstellung von L-Cystein ist noch ein weiterer Schritt erforderlich. Das Dimer L-Cystin wird durch Elektrolyse in das monomere L-Cystein reduziert.
L-Cystein
L-Cystein ist eine der 20 natürlichen Aminosäuren, die die Bausteine von Proteinen bilden. Aufgrund seiner im Vergleich zu den anderen Aminosäuren einzigartigen Sulfhydryl-Seitenkette (- SH) ist es hochreaktiv und bildet stabile Disulfidbrücken.






