疫苗生产的专家
瓦克生物技术是您首选的CDMO合作伙伴,可为减毒活疫苗、灭活疫苗、(共轭)多糖疫苗、蛋白疫苗、mRNA疫苗等各类疫苗提供工艺开发与生产服务。
疫苗创新与经验

瓦克生物技术在利用微生物宿主生产治疗众多传染病的常规疫苗的领域拥有30多年经验。我们非常荣幸能够与客户合作,将多个商业项目推向市场,以继续保护全球各地的人们。
经多年研究,我们最近成功开发出了用以生产下一代mRNA疫苗的专业技术,并在德国哈雷建成拥有4条新的mRNA专用生产线的技术中心。这个技术先进的中心作为德国抗疫应急计划的一部分,部分资金来自德国政府。
疫苗能力
疫苗类型
针对多种细菌菌株的经验
瓦克生物技术疫苗服务的主要优势
了解更多有关共轭多糖疫苗生产的信息
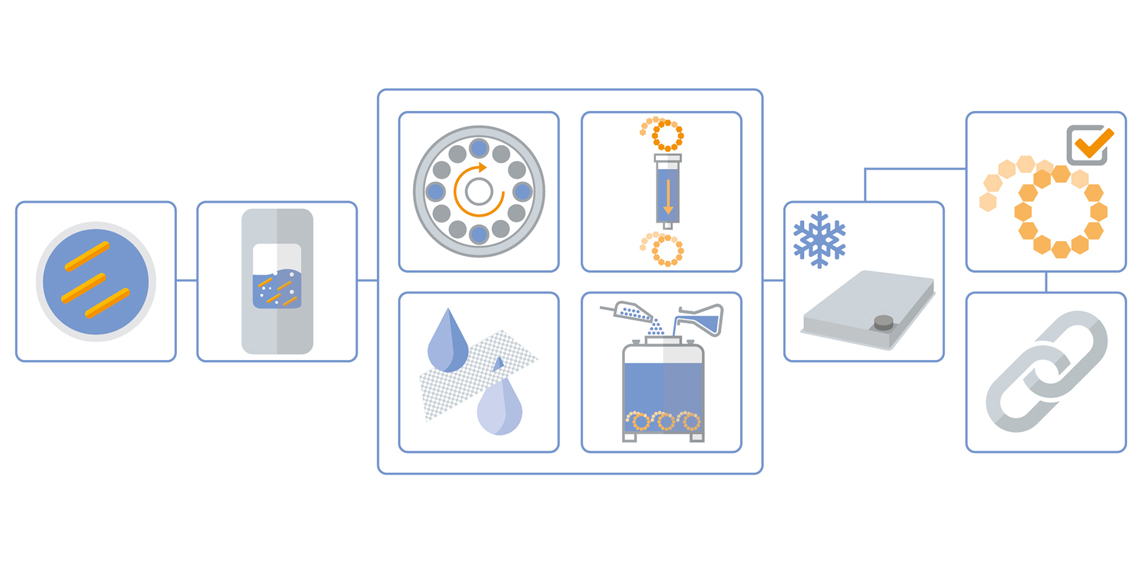
接种和预培养
用于多糖初始生产步骤的菌株由客户提供。
发酵
客户可利用瓦克生物技术经EMA/FDA认证的生产线(发酵罐容量从250升一次性反应器至1500升不锈钢反应器)调整GMP工艺规模,以满足各个项目和开发阶段的需求。
纯化
从培养液提纯多糖通常需要多个步骤,如:
• 化学灭活/热灭活后的病原体离心
• 利用超滤技术和/或深度过滤浓缩中间产物
• 使用无机盐和/或有机溶剂沉淀多糖(需防爆室和相应设备)
• 色谱步骤
冷冻干燥
将纯化的多糖和载体蛋白共轭,包括将多糖分散到LYOGUARD®承液盘中进行冻干;支持最高为65升的散料冻干。
活化
通过化学活化步骤对散装冻干多糖进行活化。
共轭
最后将活化的多糖与载体蛋白质进行化学共轭。
产品/客户聚焦
PaxVax公司的Vaxchora®产品
我们在阿姆斯特丹生产基地产出Vaxchora®口服用霍乱减毒活疫苗,供客户PaxVax公司(后被Emergent BioSolutions公司收购)商业化推广使用。20世纪70年代,霍乱注射疫苗因副作用过大而停用,口服疫苗现为预防霍乱的标准产品。
Vaxchora®2016年获美国食品药品管理局(FDA)批准,适用于2岁至64岁前往霍乱流行地区的旅行者。它是美国唯一获批的霍乱疫苗,亦获得欧洲药品管理局(EMA)批准。
霍乱弧菌是一种革兰氏阴性、兼性厌氧菌,经常会引起剧烈、致命的腹泻与呕吐。我们的先进设施极其适合在生物安全水平为二级的无菌环境中对这种细菌进行发酵。
MinervaX公司的GBS疫苗
总部位于丹麦的MinervaX公司响应世界卫生组织的号召,开发出一种针对B群链球菌(GBS)的疫苗;GBS这种细菌可能感染婴儿、孕妇和老年人/高危成年人而危及生命,也与每年50万婴儿早产有关。相应疫苗不仅能够拯救生命,还可减少对抗生素的过度使用,而过度使用抗生素会导致抗生素耐药性。
MinervaX的主要候选疫苗基于隆德大学研究成果,是一种新型的纯蛋白疫苗,由所选GBS表面蛋白中具有高度免疫原性和活性的蛋白结构域的融合构建而成。瓦克生物技术为III期临床试验提供活性蛋白成分,我们在阿姆斯特丹的疫苗卓越中心还为后期商业生产进行技术转移、工艺表征和工艺验证。
瓦克生物技术作为实力雄厚的生产合作伙伴,在后期临床和商业供应领域拥有良好业绩,我们非常期待在III期研究前与瓦克团队开展合作。
点击此处,查看我们的疫苗手册,或阅读有关我们部分疫苗合作项目的新闻稿
Brochures
借助瓦克,更上一层楼
我们期待着为您的生物制剂问世而助力。


