接种和预培养
菌株由客户提供。
18+年以来,瓦克生物技术始终是开发和生产活性微生物产品(LMP)的先锋企业。阿姆斯特丹生产基地作为我们LMP卓越中心的所在地,拥有生产含活体微生物制剂药(包括注射免疫治疗、外用药物、减毒活疫苗)的专业生产技术。
联系我们
客户可根据各项目和开发阶段的需要,获益于不同规模的GMP生产。我们提供经EMA/FDA验证的生产线,规格从250升一次性容器至1500升不锈钢罐不等。
您还将受益于我们独特的LIBATEC®平台,以及我们对各种细菌(野生型、转基因、需氧菌株、厌氧菌株)掌握的丰富经验。这些细菌可用于种类丰富的LMP,包括经美国食品药品管理局(FDA)界定的各类活体生物治疗产品。
了解更多有关LIBATEC®的信息
| 拥有对20+种不同菌株的经验和专业知识 | |||
|---|---|---|---|
| 耐氧菌 | |||
革兰氏阴性菌 |
|
|
革兰氏阳性菌 |
|
|
||
| 厌氧菌 | |||
瓦克生物技术专有的LIBATEC® (Li ve Ba cterial Tec hnology/活性细菌技术)平台实现了无保持时间生产这一处理活性生物体的核心工艺),并可在整个生产过程中确保细胞活力。该平台还完全适用于各种活性微生物菌株,以及需氧生物和特定厌氧生物的发酵工艺。
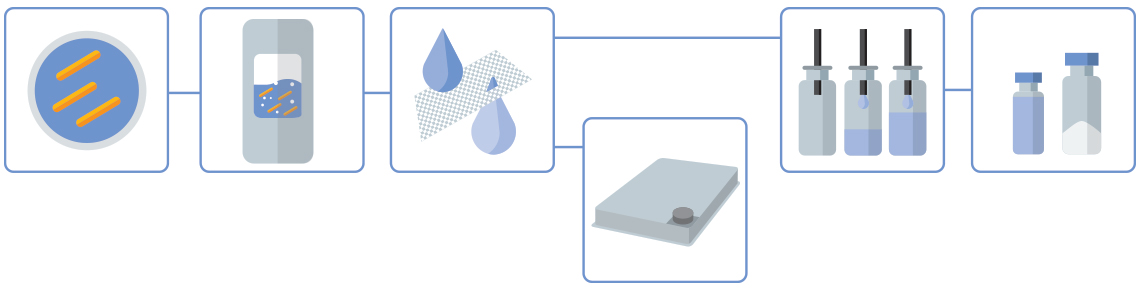
菌株由客户提供。
客户可利用瓦克生物技术经EMA/FDA认证的生产线(250升一次性发酵罐,至1500升不锈钢发酵罐),调整GMP工艺规模,以满足各个项目和开发阶段的需求。
现有离心工序通常可借助切向流过滤(TFF)被超滤/微滤步骤所取代。这也是一种一次性技术,可确保工艺在每个阶段均可保持封闭性和单菌状态。
散装原料药可分装入承液盘并冻干,支持最高为65升的散料冻干。
无菌灌装操作在瓦克生物技术的GMP灌装设备中进行,该设备有一个配方/制备区和一个主要灌装区。
可将制剂药装入小瓶,液体和冻干制剂的批量灌装可达20,000个单位(DIN 2R至20R)。
Aurealis Therapeutics股份公司请瓦克生物技术对旗下用于慢性伤口治疗的主要候选药物AUP1602-C进行工艺开发、放大和GMP生产。局部使用转基因乳酸菌,可促进慢性伤口不愈合患者的组织再生,但产品会直接接触人体组织,因此需要在单菌条件下生产。
该工艺已成功转移,适用于在GMP条件下进行单菌生产和放大。之后,在瓦克生物技术的250升一次性生物反应器中进行GMP单菌生产,并将产品无菌灌装到了每批约4000个的小瓶中。事实证明,项目开发而成的工艺极其稳定,能够产出不怕制备、保持时间及低温储存的细胞,所得制剂药的细胞活力符合规定标准(每毫升1010-1011菌落形成单位)。瓦克生物技术还对产品测试所需分析测试进行了设置、开发和验证。该制剂药已成功放行,用于I期临床试验,目前正计划进行II期试验。
我们非常高兴瓦克团队以其高超的技术能力、可靠性和大力支持让我们的主要候选药物按计划顺利进入临床——瓦克是这个项目名符其实的合作伙伴!
Juha Yrjänheikki,Aurealis Therapeutics公司CEO总部位于英国伦敦的Prokarium公司是微生物免疫疗法领域的先锋企业。瓦克生物技术正在为该公司进行一种用于治疗膀胱癌的口服生物制剂的GMP生产。Prokarium公司的产品管线充分利用癌症免疫学取得的最新突破,将癌症免疫疗法提升到一个新高度,尤其是利用转基因沙门氏菌作为输送机制,向膀胱细胞输送抗肿瘤有效载荷。
瓦克生物技术在活性微生物产品和GMP生产领域拥有深厚的专业知识,我们非常高兴能够与瓦克生物技术开展合作。
Kristen Albright,药学博士、Prokarium首席执行官